Dicht an dicht in der Zelle
Chemiker der Universität Konstanz erforschen den Einfluss der Moleküldichte in der Zelle auf die Stabilität eines Proteins auf atomarer Ebene
Welchen Einfluss hat die Umgebung einer Zelle mit ihrer dichten Konzentration an Molekülen auf die Stabilität eines Proteins? An der Universität Konstanz untersuchten die Chemikerin Birgit Köhn und Chemiker Juniorprofessor Dr. Michael Kovermann diese Frage mittels Kernspinresonanz-Spektroskopie. Ihre Ergebnisse zeigen, dass eine hohe Moleküldichte zur Stabilität des Proteins beiträgt, unabhängig von der untersuchten atomaren Position. Die Forschungsergebnisse wurden am 13. November 2020 in der Fachzeitschrift Nature Communications veröffentlicht.
Die menschliche Zelle ist ein dicht gedrängter Ort: Unzählige Makromoleküle befinden sich hier in hoher Konzentration beisammen – wie ein eng gedrängter Marktplatz, wo Menschen dicht an dicht beisammenstehen und jeder mit jedem zusammenstößt. Beim überfüllten Marktplatz ist uns klar: Die Anzahl der Personen, die auf engem Raum zusammenstehen, hat einen Einfluss auf das jeweilige Verhalten der einzelnen Menschen. Doch gilt dies auch für die Proteine in der menschlichen Zelle? Beeinflusst die Moleküldichte in der Zelle die Eigenschaften eines Proteins?
„Die meisten biochemischen und biophysikalischen Labore untersuchen Proteine in freier Lösung. Vereinfacht gesagt: Da ist ein einzelnes Protein und darum herum nur Wasser und sonst nichts“, schildert Michael Kovermann. „Wir haben uns aber zwei grundsätzliche Fragen gestellt: Ist das Protein in der dicht gedrängten Molekülumgebung der Zelle genauso stabil wie in freier Lösung? Sind alle Atome, aus denen das untersuchte Protein aufgebaut ist, in gleicher Weise vom Übergang von freier Lösung in eine dicht gedrängte Umgebung betroffen?“
Simulation hoher Moleküldichte
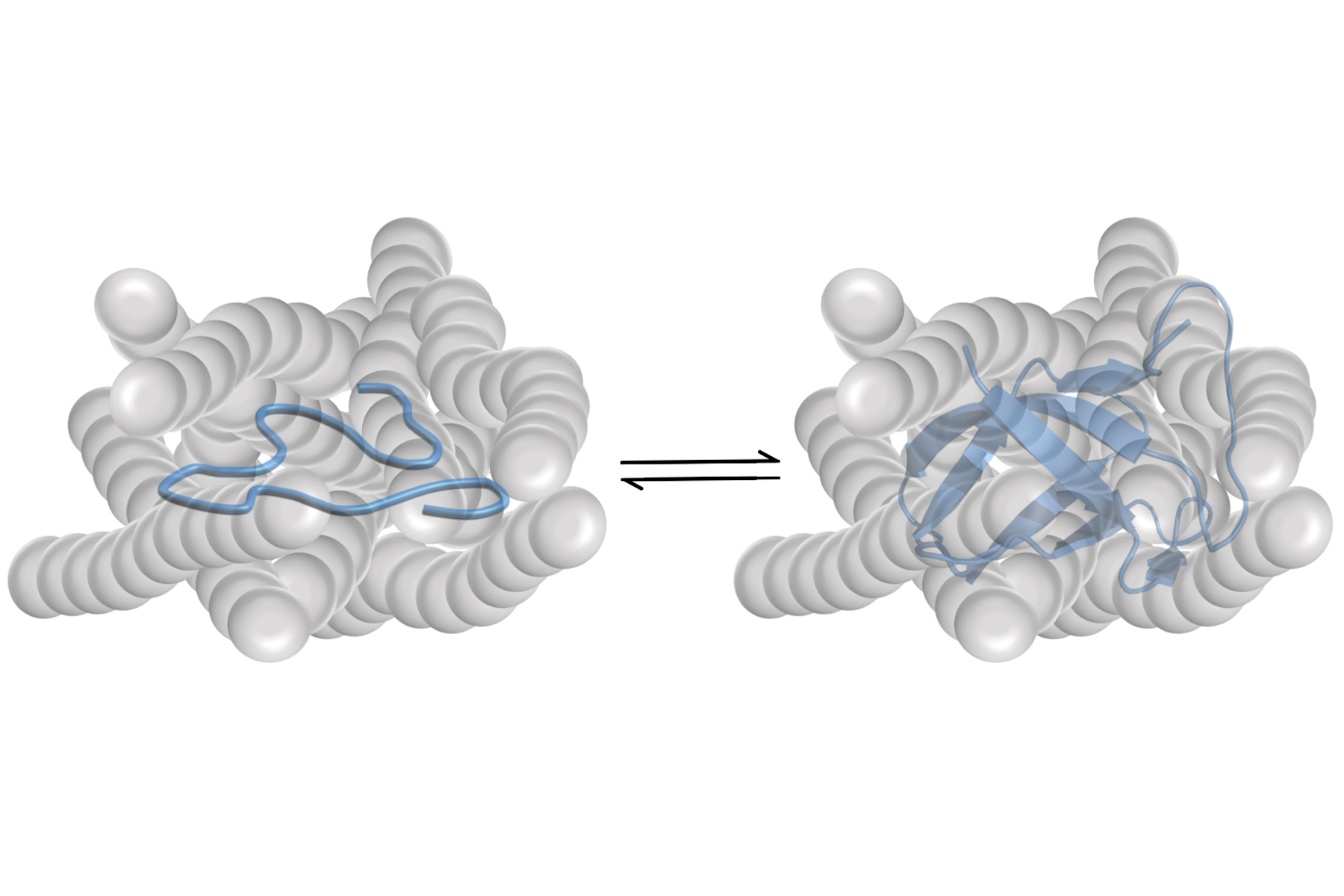
Birgit Köhn und Michael Kovermann simulierten daher die dicht gedrängte Umgebung der Zelle in einer Experimentreihe. Für das untersuchte Protein (ein sogenanntes Kälteschockprotein aus Bacillus subtilis) stellten sie folglich eine künstliche Umgebung mit einer hohen Dichte an benachbarten Makromolekülen her. Sie beobachteten dabei die Auswirkung der Moleküldichte auf die Stabilität der Faltung eines Proteins. „Das Protein ist wie eine Perlenkette beschaffen. Es hat aber die Eigenschaft, sich in einer bestimmten, charakteristischen Formation zusammenzulagern – das nennen wir seine Faltung“, führt Birgit Köhn aus: „Die Faltung ist essenziell, weil sie jedem Protein seine einzigartige Funktion verleiht. Schon die kleinste Änderung der Faltung kann große Auswirkungen auf die Funktionalität des Proteins haben.“
Ein Protein gilt als stabil, wenn es in der Lage ist, seine charakteristische Formation beizubehalten. Chemische Störfaktoren können aber dazu führen, dass ein Protein seine Formation verliert, sich also auseinanderfaltet. Welcher Effekt zeigt sich nun in der Zelle: Tragen die anderen Makromoleküle in der Zellumgebung dazu bei, dass das Protein seine Faltung aufrechterhält, oder sind sie vielmehr ein Störfaktor?
Analyse mittels NMR-Spektroskopie
Birgit Köhn und Michael Kovermann setzten Kernspinresonanz-Spektroskopie (NMR-Spektroskopie) ein, um die Auswirkungen der Zelldichte auf die Proteinfaltung zu untersuchen. Der Vorteil der NMR-Spektroskopie: Sie ermöglicht, alle Atome des Proteins gleichzeitig im Blick zu behalten. Dadurch können die Auswirkungen auf das Protein nicht nur an einer Stelle, sondern an wirklich allen Positionen des Proteins simultan untersucht werden.
„Wir haben herausgefunden, dass alle Atome des Proteins denselben Effekt zeigen: Dass das Protein in der verdichteten Umgebung signifikant stabiler ist als in freier Lösung, und zwar an allen Positionen“, spricht Birgit Köhn. „Wir entdeckten einen sehr starken kooperativen Effekt durch die Moleküldichte in der Zelle. Dieser Effekt zeigte sich unabhängig von der Wahl der ‚Crowder‘, somit unabhängig von der Beschaffenheit der Störmoleküle“, ergänzt Michael Kovermann.
„Was ungewöhnlich ist: Diese Entdeckung war nicht das Verdienst einer großen Forschungsgruppe, sondern war die beachtliche Leistung einer Individual-Promotionsarbeit“, hebt Kovermann hervor und betont: „Die sehr gute NMR-Ausstattung an der Universität Konstanz hat es uns ermöglicht, das Forschungsprojekt erfolgreich umzusetzen.“
Faktenübersicht:
- Forschungsprojekt an der Universität Konstanz untersucht mittels NMR-Spektroskopie den Einfluss der hohen Moleküldichte einer Zelle auf die Stabilität der Faltung eines Proteins.
- Das untersuchte Protein weist in einer Umgebung mit hoher Moleküldichte eine signifikant höhere Stabilität auf als in freier Lösung, unabhängig von der atomaren Position.
- Promotionsprojekt von Birgit Köhn an der Universität Konstanz in der Arbeitsgruppe von Juniorprofessor Dr. Michael Kovermann.
- Originalpublikation: Birgit Köhn, Michael Kovermann, All atom insights into the impact of crowded environments on protein stability by NMR spectroscopy, Nature Communications, 13.11.2020. DOI: 10.1038/s41467-020-19616-w
- Birgit Köhns Forschung wurde vom Young Scholar Fund der Universität Konstanz gefördert.
